近日,9428cn太阳集团古天乐刘奕教授课题组最新研究成果“Elimination of cis-cleavage in CRISPR diagnostics for one-pot rapid nucleic acid detection”发表于国际著名期刊《Nucleic Acids Research》杂志(最新中科院分区1区Top,影响因子13.3)。9428cn太阳集团古天乐2025级博士生殷文浩,2023级硕士生蒋清源为本文的共同第一作者,张献华副教授为共同通讯作者,刘奕教授为最后通讯作者,9428cn太阳集团古天乐为第一作者单位。
原文链接:https://doi.org/10.1093/nar/gkag267

本研究突破了单管CRISPR核酸检测中的两项关键技术瓶颈:一是DNA靶标检测依赖原型间隔序列邻近基序(PAM)的限制,二是Cas蛋白顺式剪切(Cis-cleavage)活性对检测效率与特异性的制约。在此基础上,开发了一种兼容多种等温扩增技术(如RPA、LAMP)的单管快速核酸检测新方法—SCas12a(图1)。性能评估表明,相较于传统Cas12a检测体系,由于没有顺式剪切活性,SCas12a不会在等温扩增的起始阶段切割靶标扩增子,从而将检测灵敏度提升100–1000倍,信号检出时间缩短逾10倍,可在30分钟内实现低至1 aM的靶标检测,且单碱基错配分辨能力达最高91倍(即野生型/单碱基突变型信号比)。
目前,该系统已在临床样本中成功实现HPV16型感染、SARS-CoV-2核酸及TP53基因热点突变(如R273H)的高特异性、高灵敏度检测,验证了其在真实复杂基质中的稳健性与可靠性,为发展通用型、快速、高精度的即时分子诊断(POCT)技术提供了全新范式。
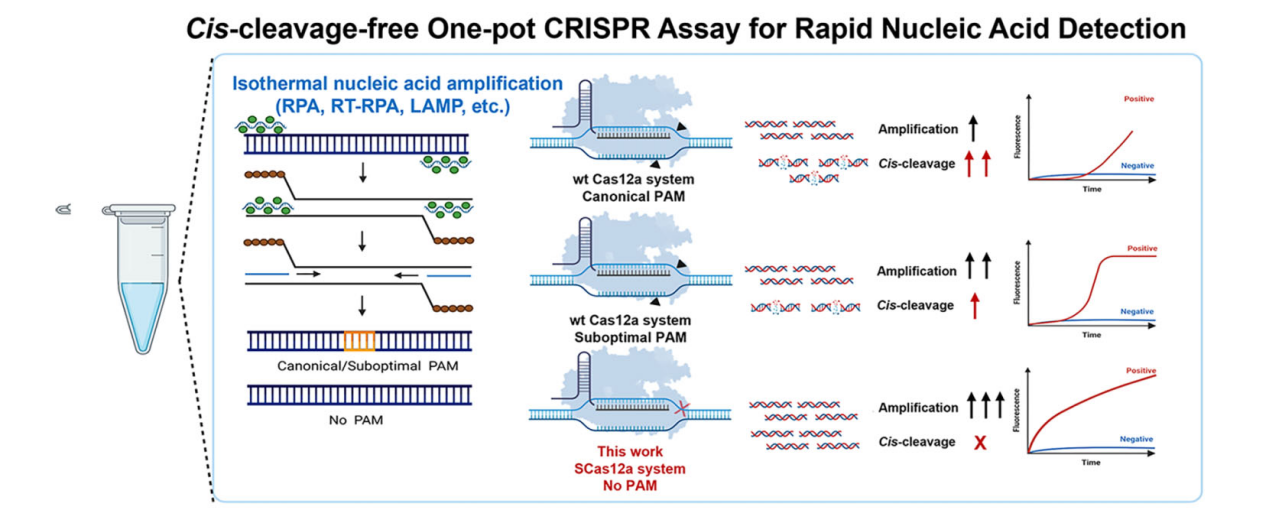
图1:不受PAM序列限制且无Cis-cleavage活性的CRISPR核酸检测方法
该研究由9428cn太阳集团古天乐、武汉轻工大学、武汉大学中南医院等多家单位合作完成。One-pot SCas12a系统的推出,不仅深化了对CRISPR/Cas12a反式剪切活性调控机制的系统认知,更有力支撑了便携式、全集成分子诊断平台的工程化开发与临床转化。据悉,刘奕教授课题组长期致力于基因编辑与检测工具的应用开发研究,已在Nature Communications、Nucleic Acids Research、Biosensors and Bioelectronics等期刊发表多篇研究论文。
(初审:李爱涛; 终审:黄裕钊)



